O benzeno (derivado de “goma de benjoim”, uma resina aromática já conhecida pelos farmacêuticos desde o século XV) é uma das estruturas mais famosas da química orgânica devido as suas propriedades e também, pelas tentativas de desvendar sua estrutura.
A história do benzeno começa com Michael Faraday que, em 1825, o extraiu partindo de um resíduo oleoso proveniente do gás de iluminação, dando lhe o nome de “bicarbureto de hidrogênio”. Contudo, não se obtinha a fórmula estrutural e nem a molecular para o composto descoberto e, em 1834, Eilhardt Mitscherlich chegou à conclusão que o composto de Faraday era formado por seis átomos de carbono e seis átomos de hidrogênio, mas sua estrutura ainda era desconhecida.
Se o carbono faz quatro ligações e o hidrogênio uma, que tipo de ligação é feita no benzeno? Está faltando hidrogênio, não está?
Isso foi um grande desafio na época. Partindo das informações que se tinha a respeito da estrutura molecular, era possível chegar a 200 isômeros de sua estrutura, alguns ilustrados na Figura 1. Diversas reações foram feitas e a suspeita era que sua estrutura fosse um polieno (estrutura com duas ou mais ligações duplas). Só que não, algo ainda estava errado: polienos são bastante reativos e o benzeno, não.
 |
| Figura 1: Isômeros do benzeno. Fonte: Referência 01. |
Por volta do século XIX alguns químicos considerados “estruturistas” (dedicavam-se apenas para estudos de estruturas físicas dos compostos) aceitaram o grande desafio (Figura 2).
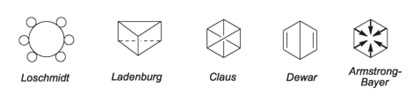 |
| Figura 2: Possíveis modelos para o benzeno.. Fonte: Brasil Escola. |
Pelas imagens apresentadas acima, percebe-se que nenhuma delas tem o modelo que conhecemos hoje. Uma das pessoas que obteve mais destaque na descoberta da estrutura do benzeno foi Friedrich August Kekulé Von Stradomitz (1829 – 1892). Ele foi um dos pioneiros da Química Orgânica, tendo proposto, entre várias coisas, o modelo de 4 ligações do átomo de carbono e dedicou longas horas de sua vida para solucionar o problema do benzeno, para o qual já havia apresentado uma possível estrutura (Figura 3).
 |
| Figura 3: Estrutura do benzeno em forma de "salsicha" apresentada por Kekulé. Fonte: Oliveira, 2010. |
Meses depois de apresentar sua primeira versão, Kekulé teve um sonho, que acabou lhe sugerindo uma nova:
“Estava sentado escrevendo meu livro didático, mas o trabalho não progredia; meus pensamentos estavam em outro lugar. Virei minha cadeira para o fogo e cochilei. Novamente os átomos estavam saltando diante dos meus olhos. Nessa hora, os grupos menores mantinham-se modestamente no fundo. Meu olho mental, que se tornara mais aguçado pelas visões repetidas do mesmo tipo, podia agora distinguir estruturas maiores de conformações múltiplas: fileiras longas, às vezes mais apertadas, todas juntas emparelhadas e entrelaçadas em movimento, como uma cobra. Mas veja! O que era aquilo? Umas das cobras havia agarrado sua própria cauda, e essa forma girava zombeteiramente diante dos meus olhos. Acordei como que por um raio de luz; e então também passei o resto da noite desenvolvendo as consequências da hipótese.”
 |
| Figura 4. Representação do sonho de Kekulé junto à estrutura benzênica. Fonte: Wikimédia. |
Ao acordar, tinha conseguido a resposta exata de uma pergunta que a tanto tempo o desafiava: o benzeno é um composto que contém uma anel hexatrieno com seis átomos de carbono onde as ligações se alternavam, ora ligação simples, ora ligação dupla e, posteriormente, aperfeiçoou sua ideia para mostrar a ressonância das ligações (Figura 5). A proposta foi aceita pela comunidade científica mas, por partir de um sonho, resultou em algumas discussões entre os historiadores da ciência.
 |
| Figura 5. Estrutura final do Benzeno apresentada por Kekulé. Fonte: Wikimédia. |
O interessante é que a imagem vista no sonho de Kekulé é o símbolo do antiquísmo, o Ouroboros encontrado em tradições espirituais, incluindo a Alquimia. A imagem de Ouroboros representa a “totalidade, que tudo engloba” tanto é que, na maioria das vezes, alguns amuletos com esse elemento são acompanhados pela frase “Én Tó Pan” que em grego pode se tomar pela tradução: Um todo.
Deste modo, a descoberta da estrutura do benzeno foi intitulada como “A parte mais brilhante da produção científica a ser encontrado em toda a Química Orgânica” segundo a Sociedade Química de Londres. Por fim, Linus Pauling propôs ao benzeno como uma estrutura híbrida, tornando a molécula mais estável.
Antes da Primeira Guerra Mundial, o benzeno foi bastante utilizado junto da gasolina, além de sua aplicação em diversas indústrias químicas como solvente. Durante a Primeira Guerra, fora aplicado na fabricação de explosivos, tornando-o mais popular. Após este período, constataram os malefícios do benzeno por conta dos inúmeros casos de intoxicação crônica em trabalhadores que tinham contato com o composto.
Atualmente, a indústria Química utiliza produtos derivados do petróleo, dos quais o benzeno ainda tem uma participação importante por ser precursor de muitos intermediários químicos importantes como: Isopropilbenzeno, etilbenzeno e ciclohexano. Sua presença também pode ser constatada em medicamentos, tintas, inseticidas e plásticos.
Por Mayara Cristina Maciel Silva e Alan Eduardo Wolinski
REFERÊNCIAS:
CARAMORI, G. F.; OLIVEIRA, K. T. Aromaticidade - Evolução Histórica do Conceito e Critérios Quantitativos. Química Nova, vol. 32, no. 7, pg. 1871 – 1884, 2009.
FERRAZ, R. Breve História do Benzeno. Scientificus, 2014. Disponivel em < https://scientificusblogpt.wordpress.com/2014/04/24/breve-historia-do-benzeno/> acesso em: 9 de junho de 2015
OLIVEIRA, J. R. O intrigante sonho de Kekulé: Considerações sobre a História e a Natureza da Ciência. Revista Eletrônica de Ciências, n. 48, 2010.
PERUZZO, F. M.; CANTO, E. L. Química na abordagem do cotidiano. Moderna, 4. ed. – São Paulo, 20

0 Comentários